CRIPSR Gene Wars: Die Ausrottung ganzer biologischer Arten und die smarte Landwirtschaft der Zukunft
Mit dem Gene Drive lassen sich Pflanzen gezielt und schnell verändern, aber auch ganze biologische Arten ausrotten oder menschliche Embryonen genetisch optimieren. Mit dem CRISPR-System geht das jetzt noch einfacher, schneller und kostengünstiger, sodass dieses neue Werkzeug ähnlich der Atomenergie Segen und Fluch zugleich sein könnte.
Gene Drive leicht verständlich erklärt
Gene Drive (engl. für Genantrieb) wird genutzt, um gezielt neue Gene in Populationen massiv zu vermehren oder im Gegenteil Gene in Populationen zu zerstören, sodass die Nachkommen beispielsweise unfruchtbar werden. Damit können zumindest theoretisch ganze biologische Arten komplett ausgelöscht werden.
Das ist im Prinzip auch schon seit 15 Jahren mit Genomeditierungsmethoden wie TALEN möglich, doch mit CRISPR geht dies nun viel einfacher, schneller und kostengünstiger, sodass prinzipiell jeder in seiner Garage zum Gentechniker werden könnte.
Bei einem Gene Drive werden die klassischen Mendel’schen Regeln der Vererbung außer Kraft gesetzt. Normalerweise werden nämlich bei der sexuellen Vermehrung je ein Chromosomensatz vom Vater und einer von der Mutter an die Nachkommen vererbt. Einzelne Gene liegen so immer in zwei verschiedenen Ausprägungen (Allelen) vor.
Welche Allele sich auf Dauer durchsetzen, hängt davon ab, ob sie der Population einen Vorteil bringen. Der Gene Drive bewirkt nun, dass immer beide Allele eines Gens identisch sind und damit bestimmte Merkmale reinerbig vorliegen (siehe Abb. 1).
Und der auf CRISPR basierende Gene Drive besteht aus einem DNA-schneidenden Enzym, das eine bestimmte DNA-Sequenz aus dem zweiten Strang eines Chromosoms ohne Gene Drive schneidet. Über eine folgende DNA-Reparatur dient der Strang mit Gene Drive als Reparaturvorlage für die geschnittenen DNA-Stränge. Dadurch kommt es zur überproportionalen Ausbreitung, denn alle Nachkommen tragen nun den Gene Drive.
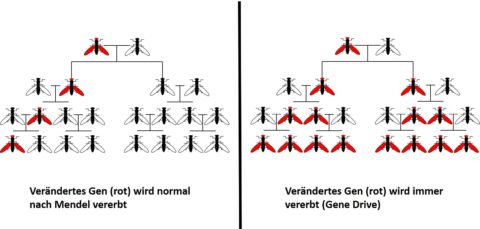
Bild: Dr. Stefan Graupner
Abb. 1: Prinzip der Mendel’schen Vererbung versus Gene Drive
Doch was macht man damit und wo liegen die erstaunlichen Potenziale dieser machtvollen Technik?
Gene-Drive-Anwendungen bei Tieren
Weltweit erkranken jedes Jahr schätzungsweise 200 Millionen Menschen an Malaria und eine halbe Million Menschen stirbt daran. In den 1950er-Jahren schon wurde in den USA die Sterile Insect Technology zur Bekämpfung unerwünschter Insektenpopulationen etwa der Anopheles-Mücke entwickelt.
Dabei werden im Labor gezüchtete Insekten durch radioaktive Bestrahlung sterilisiert und anschließend freigesetzt. Paaren sie sich mit wilden Artgenossen, bleibt der Nachwuchs aus und die Population verkleinert sich so drastisch. Die Methode wurde und wird erfolgreich eingesetzt, z. B. bei der Bekämpfung von Tse-Tse-Fliegen, Schmeißfliegen und Fruchtfliegen.
Inzwischen versuchen Wissenschaftler, die Fortpflanzung unerwünschter Insekten durch gentechnische Veränderung zu verhindern. Am bekanntesten sind die Projekte der britischen Firma Oxitec und ihre RIDL-Methode (engl. Release of Insects carrying a Dominant Lethal). Dabei wird ein Gen in das Erbgut männlicher Insekten eingeführt, das dafür sorgt, dass nach der Paarung der Nachwuchs schon im Larvenstadium stirbt. Die Bill & Melinda Gates Foundation unterstützt das Programm gegen Malaria massiv.
Bei der Ägyptischen Tigermücke Aedes aegypti, die verschiedene tropische Viren wie Dengue, Chikungunya und Zika überträgt, hat Oxitec die RIDL-Technik schon sehr weit entwickelt. Seit 2009 führte die Firma mit den gentechnisch veränderten Mücken Freisetzungsversuche durch. Bei all diesen Versuchen konnten die Mückenpopulationen um etwa 90 % verringert werden.
Brasilien hat dann 2014 als erstes Land die kommerzielle Nutzung einer gentechnisch veränderten Tigermücke zugelassen. Und nicht nur die Mückenpopulationen gingen im Versuchsgebiet deutlich zurück, sondern auch die Zahl der Dengue-Infektionen um ca. 90 %. Selbst in den angrenzenden Bezirken wurden 52 % weniger Menschen neu mit Dengue-Fieber infiziert.
Diese Art der Bekämpfung von Krankheitserregern halte ich persönlich für sehr elegant, denn auf giftige Chemikalien kann so verzichtet werden und es wird wirklich nur der Erreger selbst gezielt bekämpft.
Zudem ist die Natur ja immer schlauer, sodass es wohl nicht zur kompletten Ausrottung von Arten kommen wird. Denn durch Mutationen gibt es immer wieder Tiere, die sich dem menschlichen Gene-Wars-Angriff entziehen können und damit die Arterhaltung sichern.
Gene-Drive-Anwendungen in der Landwirtschaft
Auch für die Bekämpfung einiger Pflanzenschädlinge ist die RIDL-Technik schon weit entwickelt: So werden entsprechend gentechnisch veränderte Baumwollkapselwürmer und Kohlmotten bereits seit einigen Jahren in den USA unter freilandähnlichen Bedingungen getestet. Anfang 2017 beantragte die Cornell-Universität einen Freilandversuch mit gentechnisch veränderten Kohlmotten im Bundesstaat New York.
Wenn Krankheitserreger den Menschen selbst bedrohen, tendieren wir oft dazu, die ganze Art ausrotten zu wollen. Bei Pflanzen versuchen wir dagegen eher, nicht die Schädlinge zu eliminieren, sondern die Pflanzen selbst resistent zu machen. Und das ist bei Pflanzen meist nicht einfach, da sie oft nicht nur zwei Chromosomen, sondern 6, 8 oder noch mehr Chromosomen pro Zelle besitzen. Mit klassischen Methoden der Züchtung kommt man hier nicht weit.
Wie in Tab. 1 zu sehen, arbeiten die meisten Projekte inzwischen mit CRISPR statt mit TALEN. Neben Resistenzen gegen Krankheitserreger werden auch Allergene gezielt ausgeschaltet, der Geschmack verbessert oder gar ungesunde Nährstoffe wie Transfettsäuren eliminiert. Und meist wird das nicht unter gentechnisch veränderten Organismen (GVO) eingestuft, sodass der Verbraucher davon leider nichts weiß.
| Pflanzenart | Ziel | Verfahren | Wer? | Stand |
| Alfalfa (Luzerne) | geringerer Ligningehalt, bessere Futterverwertung | TALEN | Calyxt, S&W Seed | in den USA nicht als GVO eingestuft |
| Citrusfrüchte | Resistenz gegen Citrus Greening | CRISPR | Univ. of Florida | Projekt publiziert |
| Erdnuss | Ausschalten von Allergenen | CRISPR | Aranex, UK | Entwicklung |
| Grapefruit | Resistenz gegen Citrus-Krebs | CRISPR | Univ. of Florida | Projekt publiziert |
| Gurken | Resistenz gegen Viren | CRISPR | Volcani Center, Israel | Projekt publiziert |
| Kartoffel | Stärkezusammensetzung | CRISPR | Swedish Univ. of Agricultural Sciences | Projekt publiziert |
| Kartoffel | Lagerfähigkeit, weniger Acrylamid | TALEN | Cellectis plant sciences Inc. | in den USA nicht als GVO eingestuft |
| Leindotter | höherer Ölgehalt | CRISPR | Yield10 Bioscience | Freilandversuche, in den USA nicht als GVO eingestuft |
| Mais | Trockentoleranz | CRISPR | DuPont Pioneer | Feldversuche |
| Mais | Resistenz gegen Blattfleckenkrankheit | CRISPR | DuPont Pioneer | in den USA nicht als GVO eingestuft |
| Orangen | Resistenz gegen Citrus-Krebs | CRISPR | Citrus Research Institute, China | Projekt publiziert |
| Pappeln | Genfunktionen | CRISPR | Univ. Umea, Schweden | Forschung |
| Raps | Bessere Platzfestigkeit der Schoten (Ertrag) | CRISPR | Uni Kiel | Projekt publiziert |
| Reis | Toleranz gegen Reisbrand (Rice blast) | CRISPR | Chinese Academy of Science | Projekt publiziert |
| Reis | bessere Wassereffizienz durch weniger Spaltöffnungen (Stomata) | CRISPR | IRRI | Projekt |
| Reis | höherer Amylose-Gehalt | CRISPR | Chinese Academy of Agricultural Sciences | Projekt publiziert |
| Reis | Duftreis | TALEN | Chinese Academy of Science | Projekt publiziert |
| Sojabohnen | veränderte Fettsäuren | TALEN | Calyxt | in den USA nicht als GVO eingestuft, Feldversuche |
| Speisepilze | kein Braunwerden nach dem Anschneiden | CRISPR | Univ. of Pensylv. | in den USA zugelassen, kein GVO |
| Tomate | besserer Geschmack | CRISPR | Univ. of Florida | Projekt |
| Tomate | frühere Reife | CRISPR | Cold Spring Harbor Lab. USA | Projekt publiziert |
| Tomate | Resistenz gegen Mehltau | CRISPR | Sainsbury Lab. UK, MPI Tübingen | Projekt publiziert |
| Wachsmais | Stärke | CRISPR | DuPont Pioneer | Markteinführung 2020, in den USA nicht als GVO eingestuft |
| Weinrebe | Resistenz gegen Mehltau | CRISPR | Rutgers University New Jersey. | Projekt |
| Weizen | Mehltau-Resistenz | TALEN | Calyxt | Feldversuche, in den USA nicht als GVO eigestuft |
| Weizen | Mehltau-Resistenz | CRISPR | Chinese Academy of Science | Projekt publiziert |
| Weizen | Weniger Gluten | TALEN | Calyxt | Entwicklung |
Tab. 1: CRISPR, TALEN und Genome Editing: Beispielhafte Projekte in der Pflanzenzüchtung
Auch hier kann man dadurch auf häufig extrem giftige Chemikalien verzichten, die u. a. auch den Bienenbestand gefährden. Ich selbst nenne das smarte Landwirtschaft, denn der Einsatz von Pestiziden wird hier durch Einsatz intelligenter und gezielter Methoden auf ein Minimum reduziert.
Neben vielen Universitäten fallen in der Tabelle vor allem die Namen DuPont Pioneer und Cellectis (WKN:A0MKPR) auf. Während DowDuPont (WKN:A2DN8H) ein Chemieriese ist, ist Cellectis eher hinsichtlich seiner Krebsimmuntherapien bekannt, aber eben auch Hauptanteilseigner seiner Tochter Calyxt (WKN:A2DU9F), die das Genomeditierungs-Know-how von Cellectis in die Landwirtschaft bringt. Und Monsanto (WKN:587919) wird hier sicher bald auch massiv mitmischen. Aber es kommt noch besser, denn der Mensch ist auch schon Ziel der Genomeditierung.
Optimierung von Embryonen
Forscher der Oregon Health and Science University in Portland haben erstmals einen erblichen Gendefekt schon in der befruchteten Eizelle repariert. Die Forscher gaben jeweils ein Spermium eines an hypertropher Kardiomyopathie erkrankten Mannes in eine gesunde Eizelle. Gleichzeitig injizierten sie die Genschere CRISPR-Cas9 in die Eizelle, die die DNA an der mutierten Stelle aufschneiden sollte.
Die Genreparatur fand so schon vor der ersten Zellteilung des Embryos statt. Dies verhindert die Entstehung von Embryonen mit nur zum Teil reparierten Zellen. Das Ergebnis: 42 der 58 Embryonen in der Studie trugen die krankhafte Mutation nicht mehr, das entspricht rund 72 %. Die Embryonen wurden dann nach wenigen Tagen zerstört, da es sich nur um ein Experiment handelte.
Durch Einführung von Gene Drives in befruchtete Eizellen ließe sich aber die Menschheit in der Theorie tatsächlich genetisch optimieren. Allerdings würde das sehr lange dauern, denn man müsste zunächst einmal Tausende von Embryonen mit Gene Drives ausstatten, die sich dann über viele Generationen erst ausbreiten würden. Aber je mehr Embryonen mit Gene Drives ausgestattet wären, desto schneller ginge es. Mein Buchtipp an dieser Stelle: Brave New World von Aldous Huxley.
Fazit
Gene Drives ermöglichen,
- Krankheitserreger gezielt auszuschalten und auf Pestizide zu verzichten,
- smarte Landwirtschaft ohne Pestizide.
Gene Wars gegen Krankheitserreger und Schädlinge sind längst Realität und haben durch zielgenaue Wirkung und Reduzierung von Pestiziden aus meiner Sicht absolute Berechtigung und Notwendigkeit.
Genome Editing per se wird viele angeborene Gendefekte heilen können, und CRISPR-Unternehmen wie Editas Medicine (WKN:A2AC4K), Intellia Therapeutics (WKN:A2AG6H) und CRISPR Therapeutics (WKN:A2AT0Z) sind hier an vorderster Front. Aber auch eine genetische Optimierung von Embryonen ist möglich, was aus ethischer Sicht zumindest fragwürdig ist. Und wer weiß, ob nicht Staaten wie China damit anfangen werden?
Nicht zittern – handeln! Der Bärenmarkt-Überlebensguide für Börsenkrisen
Der Aktienmarkt ist derzeit wieder höheren Risiken ausgesetzt. Droht vielleicht sogar ein Bärenmarkt? Vielleicht – aber steck jetzt bloß nicht den Kopf in den Sand!
Wenn die Märkte schwanken und die Nerven flattern – genau dann zählt es, wie du dich als Anleger verhältst. Unser Bärenmarkt-Überlebensguide zeigt dir in vier Schritten, wie du klug, ruhig und strategisch durch jede Korrektur kommst – und sie vielleicht sogar zu deiner größten Chance machst.
Jetzt lesen und vorbereitet sein, wenn andere in Panik verfallen!
Stefan Graupner besitzt keine der erwähnten Aktien. The Motley Fool besitzt Aktien von CRISPR Therapeutics. The Motley Fool empfiehlt Editas Medicine.